Бобровский М.А. – врач, терапевтическое отделение ИВЦ МВА
Резюме:
В статье приведены результаты исследования регенераторного действия холодной гелиевой плазмы на модель условно-асептической раны у крыс. В исследуемой группе, обработка ран холодной плазмой привела к уменьшению сроков регенерации и увеличению скорости эпителизации ран. Выводы, сделанные из результатов исследования, позволяю рассматривать холодную плазму как альтернативный метод лечения ран у мелких домашних животных.
Введение:
Плазма - ионизированный квазинейтральный газ, содержащий свободные электроны, положительно и отрицательно заряженные ионы[7]. В простом понимании, плазму принято делить на низкотемпературную (106<К) и высокотемпературную (>106К), а также на равновесную и неравновесную[11]. Исходя из того, что основным механизмом в равновесной плазме является тепловое сжигание, требующее высокой температуры рабочего газа, широкого применения в медицине, в отличии от неравновесной, она не находит.
Холодная неравновесная плазма атмосферного давления имеет ряд специфических, физических свойств оказывающих выраженный бактерицидный и биостимулирующий эффект[8]. Эти свойства можно успешно использовать для контроля течения раневого процесса у животных[9].
Методами планиметрии изучить в рандомизированном контролируемом исследовании регенеративное действие низкотемпературной, неравновесной гелиевой плазмы атмосферного давления на стандартной модели условно-асептической раны у крыс.
В исследовании использовались 30 аутбредных крыс линии Wistar в возрасте 8 месяцев - 15 самок со средним весом 148 (±13,559) грамм и 15 самцов со средним весом 179.4 (±12,654) грамм. После разделения животных на две группы в зависимости от половой принадлежности, и первичной произвольной нумерации животных в каждой группе от 1 до 15, была проведена рандомизация средствами программы “Biostat”. После этого в программе “Biostat” применен алгоритм формирования случайных выборок с распределением животных в одну из трех групп, по 10 животных (5 самок и 5 самцов) в каждой (Таб.1.). В каждой группе проведена произвольная нумерация животных по порядку от 1 до 10.
|
|
Группа №1 |
Группа №2 |
Группа №3 |
|||
|
|
Самки |
Самцы |
Самки |
Самцы |
Самки |
Самцы |
|
ср. |
144,4 |
175 |
147,8 |
180,8 |
151,8 |
182,4 |
|
ст.откл. |
±16,1 |
±17,1 |
±10,7 |
±11,1 |
±15,4 |
±10,3 |
|
ст. ошиб.ср |
±7,18 |
±7,668 |
±4,8 |
±4,954 |
±6,8731 |
±4,6 |
Таб.1 Распределение веса животных по группам (гр).
В проведенном исследовании обработка ран и проведение контрольно-измерительных работ со статистической обработкой полученных результатов независимо друг от друга занимались два разных исследователя одной исследовательской группы. Тем самым осуществлялось ослепление проведенного исследования.
Моделирование условно-асептических ран осуществлялась посредством формирования полнослойной кожной раны. С этой целью животным внутримышечно вводилось 2,5мг тилетамина и 2,5мг золазепама. После анальгезии произведено удаление шерсти и обработка кожи дорсальной поверхности грудного отдела позвоночника каудальнее лопаток семидесятипроцентным раствором этилового спирта и спиртовым раствором йода. Скальпелем №11 сформирована равносторонняя рана с образованием поверхностного кожного дефекта. Все раны обработаны 0,01% раствором бензилдиметил-миристоиламино-пропиламмония хлорида моногидратом.
Первая группа животных (группа №1) обрабатывалась холодной гелиевой плазмой атмосферного давления с расстояния 1см в течение трех минут один раз в день; вторая группа (группа №2) обрабатывалась тремя миллилитрами 0,05% раствором хлоргексидина два раза в день; третья группа (группа №3) – группа плацебо, обрабатывалась 0,9% раствором натрия хлорида, один раз в день.
Содержание животных регламентировалось нормами нормам СП 2.2.1.3218-14. Исследование проводилось в соответствии с принципами Европейской конвенций о защите лабораторных животных, международными рекомендациями по проведению медико-биологических исследований с использованием животных, ГОСТ 33044-2014, приказом МО № 742 от 13.11.84 «Об утверждении правил проведения работ с использованием экспериментальных животных» и другими нормативными документами [3,4,5,6].
Для формирования факела неравновесной плазмы, использовался аппарат “Гелиос” ТУ 9444-001-46807972-2015. В качестве газовой смеси использовался гелий марки ”Б”.
Оценка регенерации ран осуществлялась методом планиметрии. Планиметрические измерения осуществлялись модифицированным методом Л.Н.Поповой: путем переноса контуров ран на полиэтиленовые гибкие пластины перманентным маркером. Полученные пластины сканировались поверх стандартного листа А4 с нанесенной на него миллиметровой сеткой. Расчетно-аналитические работы производились с помощью программы “ImageJ” посредством обработки полученных изображений и определения площади и периметра полученного контура ран.
Для оценки регенерации использовались показатели величины периметра и площади поверхности ран. Для расчета скорости регенерации раны использовались показатели процента уменьшения площади раневой поверхности за сутки по отношению к предыдущему результату [1](Рис.2.) а также средняя линейная скорость регенерации раны, показатель которой вычислялся по методу предложенным Осицевым Е.Ю. и Солободской А.Б. (Рис.3.).
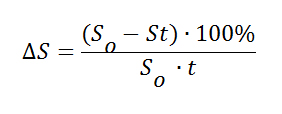
Рис.2 Формул вычисления процента уменьшения площади раневой поверхности за сутки по отношению к предыдущему дню. Где Sо - площадь раневой поверхности при предшествующем измерении; St - площадь раневой поверхности через промежуток времени t.
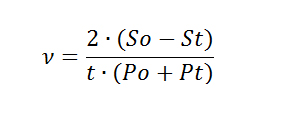
Рис.3 Формула расчета средней скорости регенерации раны. Где Pо и Sо - периметр и площадь раневой поверхности при предшествующем измерении; Pt и St - периметр и площадь раневой поверхности через промежуток времени t.
Статистическая обработка полученных результатов осуществлялась программой “Biostat” посредством получения данных описательной статистики и однофакторного дисперсионного анализа.
Анализ результатов проведённого исследования позволяет установить уменьшение сроков регенерации ран, обрабатываемых холодной гелиевой плазмой атмосферного давления в среднем на 5(±1) дней раньше в сравнении с группами №3 и №2 (Рис.1,2). Приемлемый уровень статистической значимости полученных данных наблюдался на пятый день исследования.
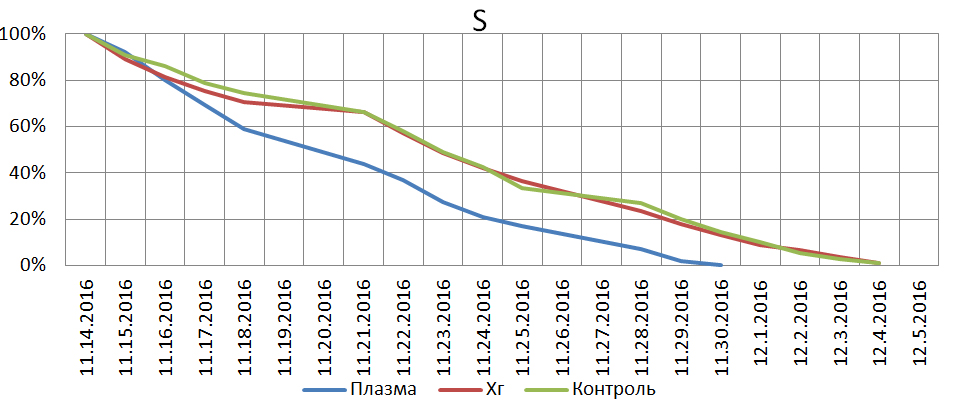
Рис.2. Относительная, средняя убыль площади поверхности ран.
*18.11.16 - р=0.04.
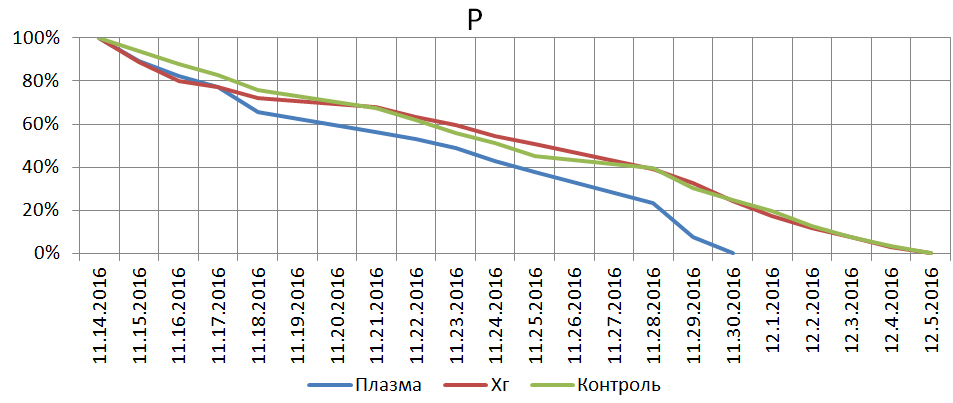
Рис.3. Относительная, средняя убыль периметра раны.
*18.11.16 - р=0.04.
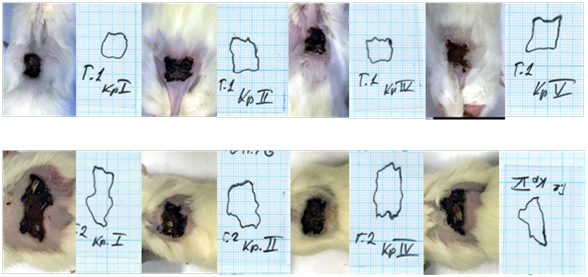
Нами был учтен тот факт, что после формирования полнослойных кожных дефектов контуры ран у разных крыс во всех группах сильно изменились, что было связано с высокой степенью эластичности кожи этого вида животных. Изначально мы получили раны различной площади и периметра (рис.4.). Для учета различия в регенерации ран различной площади нами была рассчитана средняя линейная скорость регенерации, которая показывает, какую площадь в среднем за день покрывает эпителий, растущий с единицы длины контура. Этот показатель учитывает изменение как площади, так и периметра раны. Полученная величина также покажет, с какой средней скоростью движется эпителиальный край раны по направлениям, перпендикулярным контуру раны.
|
|
Среднее |
Ст. отклонение |
Ст. ошибка среднего |
||||||
|
Группы |
№1 |
№2 |
№3 |
№1 |
№2 |
№3 |
№1 |
№2 |
№3 |
|
S̅ (мм) |
208,68 |
212,88 |
214,00 |
40,12 |
47,55 |
34,28 |
12,69 |
15,04 |
10,84 |
|
P̅ (мм) |
69,96 |
73,77 |
69,49 |
11,73 |
8,70 |
6,81 |
3,71 |
2,75 |
2,15 |
Рис.4. Различия формы и площади ран у крыс внутри групп и между ними в начале исследования.
Оценивая данные по уменьшению площади ран относительно предыдущих измерений, можно наблюдать умеренную динамику снижения площади ран в группе №1, по сравнению с группами №2 и №3, в среднем на 7% в день за первые четыре дня исследования. Последующие наблюдения показывают, что в группе №1 сохраняется общая положительная динамики уменьшения площади, превосходящая аналогичные показатели в группах №2 и 3, в течение большей части времени проводимого исследования, с максимальным значением на шестнадцатый день (разница от предыдущего измерения до 51%) (Рис.6). Данные наблюдения подтверждаются высокими значениями средней линейной скорости регенерации в группе №1 по сравнению с группами №2 и 3 (Рис.5).
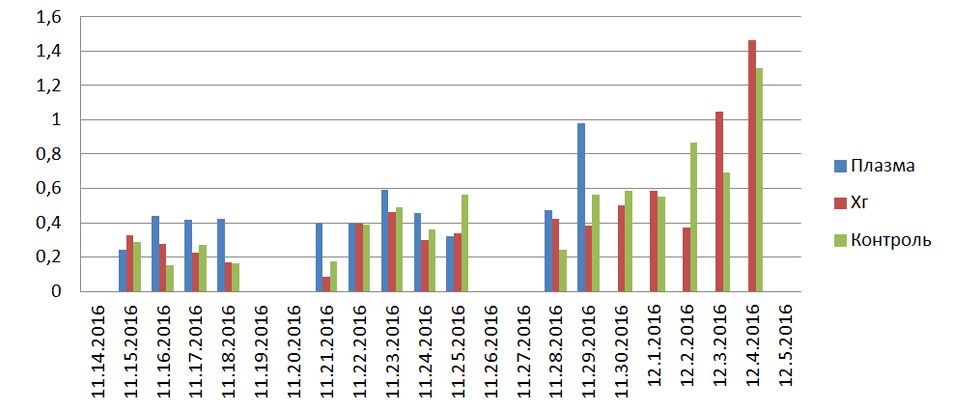
Рис.5. График средней линейной скорости заживления ран (мм/сутки).
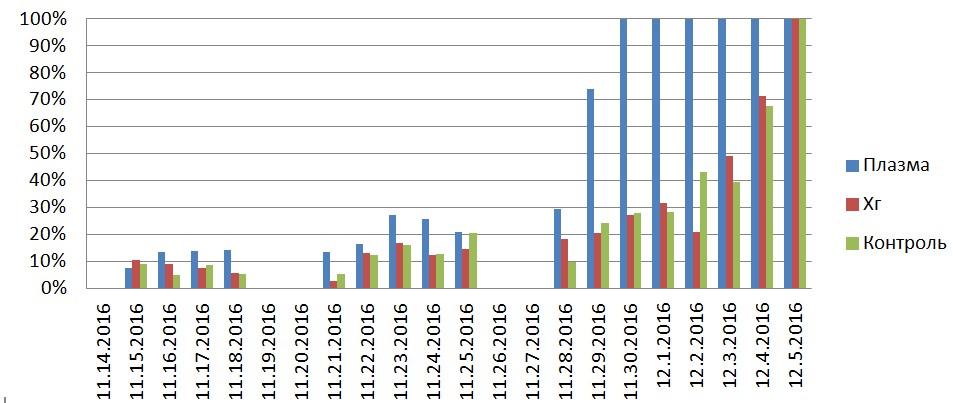
Рис.6. График уменьшения площади поверхности ран за сутки от предыдущего (%).
Отсутствие значимой разницы между группами №3 и №2 по срокам регенерации, средней линейной скорости регенерации и по уменьшению площади поверхности ран нами объясняется видом выбранной модели, а именно модель условно-асептической раны. Данные модели, как правило, не осложняются септическими процессами, поэтому степень антисептического эффекта применяемых растворов не сильно сказалась на скорости регенерации ран.
Проводя оценку регенераторной способности холодной гелиевой плазмы атмосферного давления, изученной методами планиметрии на модели условно-асептических ран у крыс, нами установлено уменьшение сроков и увеличение скорости регенерации тканей в сравнении с контрольной группой-плацебо, и группой-сравнения. Результаты исследования, соответствуют уровню доказательности 2С. Полученные данные позволяют рассматривать холодную плазму атмосферного давления, как альтернативный метод лечения ран у мелких домашних животных.
Список литературы: